![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
59 Cards in this Set
- Front
- Back
|
Hvilke primære test kan der laves? |
Gramfarvning KOH Motilitetsagar Fasekontrasmikroskopi VLFH Cytochromoxidasetest Katalaseprøve O/F-test NA vækst MacConkey Nitratmedium og nitrat reduktion |
|
|
Hvilke sekundære test kan der laves? |
|
|
|
Beskriv nigrosin-præparat |
Hvordan?Afsæt en lille dråbe nigrosin på objektglas. Koloni påføres derpå og udrøres. Lufttørring Hvad?Negativ farvning af bakterier. Alt hvad der ikke er bakterier farves med blæk. Resultat?Farvestoffet trænger ikke ind i bakteriecellen, men danner en sort hinde mellem cellerne. Der kan herudfra bedømmes om det er kokker eller stave. |
|
|
Eksempel på nigrosin-præparat |

|
|
|
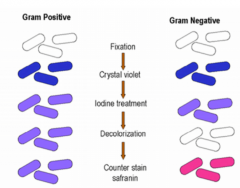
Gramfarvning |
Hvordan? Objektglas dyppes i methylviolet 1 minut. Skylles med vand. Lugols opløsning 1 minut. Skylles med vand. 99% ethanol 20 sek. Skylles med vand. Safranin 30 sek. Skylles med vand og overskydende vand kan fjernes med filtrerpapir. Lufttørring. Hvad?Binding af methylviolet til sure grupper i bakteriecellen, kan præcipitere i et kompleks med jod, som danner et sortblåd præcipitat. Dette lader sig udtrække med alkohol i G-, og farves blå i G+. Resultat?G+: BlåG-: RødeKokker?Stave?Endosporer (ufarvet legeme i cellen)? |
|
|
Eksempel på gramfarvning |
|
|
|
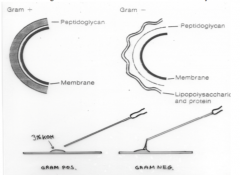
Kaliumhydroxidprøve (KOH) |
Hvordan?2 dråber 3% KOH på objektglas med afstand. Kolonimasse oprøres. Hvad?Gramfarvbarhed ved slimdannelse. Resultat?G+: mangel på slimdannelse (pga stor peptidoglycan lag i cellevæg)G-: slimdannelse (cellevæg nedbrydes og DNA frigives —> slimdannelse) |
|
|
Eksempel på KOH |
|
|
|
Kulturel bevægelighedsprøve |
Hvordan?En flamberet podenal med kultur dyppes 1cm ned i halvflydende agar. Hvad?Bakterie med eller uden flageller. Resultat?Bevægelig: Frembringer en skyet uklarhed i glasset. Ubevægelig: Kun vækst i stikkanalen |
|
|
Bevægelighdesprøve mikroskopisk |
Hvordan?Kultur i flydende medium. Kultur anbringes på objektglas. Dækglas pålægges. Fasemikroskopi udføres nu.
Hvad?Kigger efter celler der bevæger sig i alle retninger. 1 retning løber de bare med agaren.
Resultat?Bevægelig: Ubevægelig: |
|
|
VL halvflydende medium (VLHF)
(Aerob og anaerob vækst) |
Hvordan?Med udrettet podenål podes kultur i rør med VLHF til bunds. Hvad?Kan bakterien vokse med eller uden ilt. Resultat? se billeder |
|
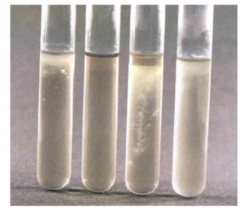
|
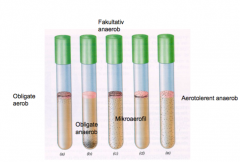
Obligat aerobt: hvis bakterien kun kan vokse i overfloden Anaerob vækst: Hvis bakterien kun kan vokse i bunden er den obligat anaerob |
|
|
Behov for ekstra CO2-test |
Hvordan?Hvis bakterien kan vokse på agarmedium i almindelig atmosfære har de ikke krav på ekstra CO2.
Hvad?Capnofile bakterier kræver 5-10% CO2. Resultat?Ekstra CO2: |
|
|
Cytochromoxidaseprøve |
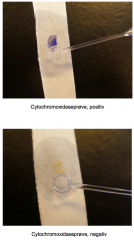
Hvordan?Oxidasereagens dryppes på filtrerpapirstrimmel. Podenål med kultur påsmøres. Aflæses efter 10 sek. Hvad?Cytochrom C påvises. Resultat?Positiv ved blå farve efter 10 sek |
|
|
Eksempel på cytochromoxidaseprøve |
|
|
|
Katalaseprøve
|
Hvordan?Kultur afsættes på objektglas. Dryppes med 3% H2O2. Aflæses for luftbobler. Hvad?Har bakterien katalase og kan den derved spalte H2O2 til ilt og vand. Resultat?Luftbobler: Katalase positiv |
|
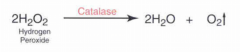
Eksempel på katalaseprøve |

|
|
|
Oxidation/fermentation prøve
|
Hvordan?Der podes til bund med kultur i O/F glukosemedium. Hvad?Kan bakterien omsætte glukose fermentativt/oxidativt ved anaerobe og aerobe forhold. Resultat? |
|
|
Eksempel på OF-prøve |

|
|
|
Vækst på nutrient agar (NA)
|
Hvordan?NA-agar inddeles i 2 felter. Stammerne podes i hvert felt 1 cm streg. Aflæses for vækst. Hvad?Kan stammerne vokse på NA-agar. Resultat?Vækst: Ikke vækst: |
|
|
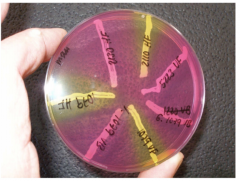
Vækst på MacConkey agar |
Hvordan?MacConkey-agar inddeles i 2 felter. Stammerne podes i hvert felt 1 cm streg. Aflæses for vækst. Hvad?Kan stammerne vokse på MacConkey-agar. Det er selektivt og indikativt medie der anvendes til påvisning af coliforme bakterier (der lever i tyktarmen) samt differentiering af Enterobacteriaceae Resultat?Vækst: Ikke vækst: |
|
|
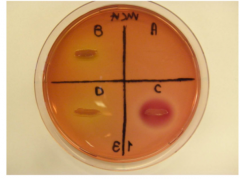
Eksempel på MacConkey agar Selektivt princip: Natriumtaurokolat og krystalviolet virker inhibitivt på defleste Gram-positive bakterier. Enterobacteriaceae er galderesistente. Indikativt princip: Natriumtaurokolat omdannes ved laktoseforgæring tiltaurokolsyre, der danner komplekser med neutralrødt. Neutralrødt erendvidere en indikator, som er rød ved en pH < 6,8 og gul ved en pH > 8,0. |
|
|
|
Nitratreduktion
|
Hvordan?Podes kultur i nitratmedium. Dagen efter tilsættes 1 ml Nit A reagens og 1 ml Nit B reagens (første trin). Ved ingen rødfarvning tilsættes zinkpulver og glasset observeres efter 10 min. Hvad? Nitrat kan udnyttes af bakterier på 2 forskellige måder. Dels optager nogle bakterier et kvælstof fra nitratmolekylet som anvende i biosyntesen. Dels kan nogle bakterier anvende nitratmolekylets ilt ved en anaerob respiration. Resultat?Rød farve første trin: Nitrit til stede |
|
|
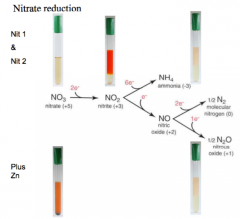
Eksempel på nitratreduktion Ved en nitratreduktionsprøve kan man påvise følgende 3 muligheder:
1. Ingen påviselig reduktion af nitrat. 2. Nitrat reduceres til nitrit, som ophobes. 3. Nitrat reduceres ud over nitrit. Ved dette tilfælde kan man evt. Vise, omslutproduktet er en luftart (læs: N2 eller N2O) ved at benytte et Durham-rør. |
|
|
|
Hvilke sekundære test findes der? |
Koagulaseprøve
Mannitol saltagar ONPG Aeskulin-blodagar Aeskulin-bouillon Xylose-rhamnose bouillon Durhamrør Skråserum Æggeblommeagar Sulfitjernagar Indol MR/VP Methylrødt prøve Voges proskauer prøve Simmons citrat Ureasemedium Ureaseenzymtest |
|
|
Koagulaseprøve
|
Hvordan?Kultur podes i bouillon. Aflæses for koagulation efter 4 og 24 timer, da stafylokokker kan producere fibrinolysin som atter kan bringe det koagulerede plasma på flydende form. Hvad?Stafylokokkers evne til at koagulere stabiliseret plasma. Resultater?Koagulation: |
|
|
Eksempel på koagulaseprøve |

|
|
|
Mannitol saltagar
|
Hvordan?Der podes med kultur på agar.
Hvad?Selvektivt og indikativt medium for stafylokokker. Den høje saltkoncentration på 7,5% hæmmer mange andre bakterier. Resultater?Vækst: Ikke vækst: |
|
|
Eksempel på mannitol saltagar Selektivt princip: Den høje saltkoncentration på 7,5 % hæmmer de flestebakterier med undtagelse af Stafylokokker, der er saltresistente. Indikativt princip: Staphylococcus aureus er mannitol-fermenterende.Under fermenteringen dannes syre, der medfører gult farveomslag af pH-indikatoren fenolrødt. Staphylococcus pseudintermedius ermannitolnegativ, dvs. Der forekommer intet farveomslag af fenolrødt. |
|
|
|
ONPG
|
Hvordan?Kultur overføres til rør med sterilt vand. Med steril pincet tilsættes ONPG-tablet. Hvad?ONPG spaltes til en gulfarvet nitrophenol af enzymet beta-galactosidase (lactase), der dannes af Staphylococcus pseudintermedius men ikke dannes af Staphylococcus aureus.
Resultater?Har laktase: Staphylococcus pseudintermedius |
|
|
Eksempel på ONPG |

|
|
|
Eskulin blodagar
(CAMP-test og bouillon) |
Hvordan?CAMP: Der podes med beta-toksisk Staphylococcus aureus som diameter. Vinkelret herpå stregpodes med kultur startende væk fra diameteren og ind mod den uden at berøre denne. Bouillon: Med udrettet podenål berøres kultur som derefter berører bouillonen.
Hvad?CAMP: Eskulin fluorescerer med blålig farve og eksulinhydrolise viser sig ved at manglende fluoroscens omkring kolonier. Desuden vil eskulinpositive kolonier vise en let brunfarvning fordi spaltningsproduktet eskulin er svagt brunfarvet. Bouillon: Ved positiv sortfarvning skyldes det udfældning af eskuletin med ferricitrat. Resultater?Fluorescens: Sortfarvning: |
|
|
Eksempel på eskulin blodagar |
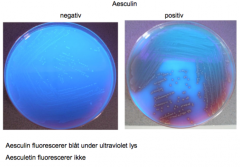
Aflæsning: Æskulin-blodagaren aflæses under UV-lys. En positiv test viser sigsom manglende fluorescering ved bakteriekolonierne, dvs. bakteriestammen harhydrolyseret æskulin til æskulitin. |
|
|
Eksempel på eskulin bouillon |

Aflæsning: Der aflæses for sortfarvning, som skyldes, at æskulitinudfældes med ferricitrat til et sort jernkompleks. |
|
|
Kulhydratmetabolisme (xylose- og rhamnosebouillon)
|
Hvordan?Med podenål berøres kultur, som herefter berører bouillon. Hvad?Bakteriel nedbrydning kan ske fermentativt eller oxidativt. Fermentativt: syredannelse i både anaerobe og aerobe del af mediet Oxidativ: syredannelse i den aerobe zone øverst i mediet.
Resultater?Fermentativ:Oxidativ: |
|
|
Eksempel på kulhydratmetabolisme |

|
|
|
Skråserum (Loeffler serum)
|
Hvordan?Kulturen berøres og føres til bunds i glasset uden at berøre mediet. På bunden berøres mediet og zig-zagges tilbage så mediets overflade podes. Der aflæses for proteolyse, der vil vise sig ved en udhuling af mediet under vækststregen. Hvad?Undersøgelse af bakteriers proteolytiske egenskaber overfor serumproteiner. Resultater?Proteolyse: |
|
|
Eksempel på skråserum |

|
|
|
Æggeblommeagar
|
Hvordan?Der podes en diameter på mediet. Hvad?Påvisning af lecithinaseproduktion hos bla. Bacillus cereus, visse klostriumarter og Staphylococcus aureus. Resultater? Vækst: Ikke vækst: |
|
|
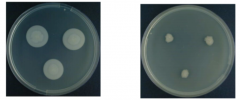
Eksempel på æggeblommeagar Indikative princip: Lecithinspaltende bakterier fraspalter fedtsyrer, derfremtræder som en hvid præcipitationszone omkring kolonierne. |
|
|
|
Sulfitjernagar
|
Hvordan?Med udrettet podenål podes ved stik til bunds. Hvad?Sulfitreduktion forekommer hos Clostridium og hos Salmonella. Reduktion af sulfit til H2S, vil reagere med Fe+++ under dannelse af sort FeS, der udfælder. Resultater?Udfældning: |
|
|
Eksempel på sulfitjernagar Indikativt princip: Sulfit reduceres til H2S, som reagerer medtilstedeværende Fe+++, hvorved der dannes sort, uopløseligt FeS - dettefælder ud i og omkring de sulfitreducerende kolonier. |

|
|
|
Indoltest
|
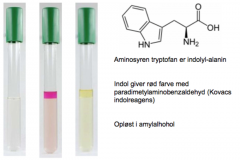
Hvordan?Podes i kødvandspeptonbouillon, og tilsættes Kovacs indolreagens. Ved let omrystning ekstraheres indol i amylalkohollaget, der lejrer sig øverst i glasset og udvikler en rød farve. Ved negativ reaktion forbliver det gult.
Hvad?Aminosyren tryptofan kan fraspaltes alanin-sidekæden under dannelse af indol. Resultater?Rød farve: Positivt - bakterien kan fraspalte tryptofanGul farve: Negativt |
|
|
Eksempel på Indol-test |
|
|
|
Methylrødt & Voges Proskauer (MRVP)
|
Hvordan? Podes med bakteriestamme og inkuberes Hvad? Anvendes til bestemmelse af slut-pH i et glukose-fosfat-medium.
Resultater? Den udvoksede kultur tilsættes nogle dråber af pH-indikatoren methylrødt. Hvis substratets slut-pH < 5, fremkommerder en rød farve (læs: methylrødt-positiv), mens svageresyredannende bakterier viser en gul farve (læs: methylrødt-negativ). |
|
|
Eksempel på MRVP |

|
|
|
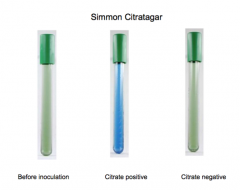
Simmons citrat agar
|
Hvordan?Zig-zag podning på overfladen. Hvad? bestemmelse af evne til at udnyttet citrat som eneste kulstofkilde og ammoniumioner som eneste kvælstofkilde Resultater? se billede |
|
|
Eksempel på simmons citrat agar |
|
|
|
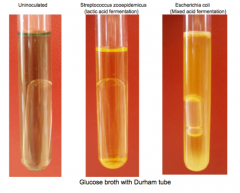
Luftproduktion - Dunhamrør (gas fra glucose)
|
Hvordan?Opsamling af luft i minireagensglas (Durhamrør), anbragt med bunden opad i rør med glukosebouillon. Hvad?Kan bakterien producere brint? CO2 opløses i vand. Resultater?Luftproduktion: |
|
|
Eksempel på Dunham-rør |
|
|
|
Urinstof bouillon
|
Hvordan? Der podes to medier med kolonimasse. Et testmedie og etkontrolmedie. Disse inkuberes ved 37 °C og aflæses efter et døgn. Testmedietvil vise basisk omslag ved rødfarvning.
Hvad? Anvendes som særligt led i identifikation af proteus der er urease-positiv
Resultater? Ureaseproducerende bakterier vil i et urinstofholdigt medium spalte urinstoffettil CO2 og NH3, hvilket fremkalder en basisk reaktion, som kan vises vedrødfarvning af pH-indikatoren fenolrødt. |
|
|
Eksempel på urinstof-bouillon |
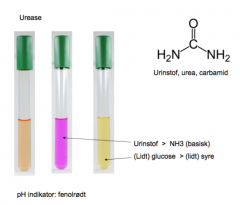
Kontrolmediet er lig testmediet, dog indeholder det ikke urinstof.Kontrolmediet vil vise en sur reaktion (læs: gul farve), hvis bakterien erglukosefermenterende og eller en neutral, rødgullig farve. |
|
|
Müller Hinton salt-polymyxin bouillon (MHSPB)
|
Hvordan?Dag 1 —> Svaber fugtes i rør med sterilt isotonisk saltvand. Afsvabring af slimhinde i vestibulum nasi. Svaber deponeres i rør med MHSPB og den frie del afknækkes sådan at den kan være i røret. Inkubation 37 °C. Dag 2 —> Podning på blodagar med øjepodenål. Inkubation 37°C. Hvad?Saltbouillon er selektivt for flydende opformering af Staphylococcus pseudintermedius og S. aureus. Polymoxin er selektivt for gram + bakterier. Resultater? Ingen i gruppen havde Staphylococcus aureus. Kan kendes ved dobbelthæmolyse og gule kolonier. |
|
|
Macfarland, Muller Hinton agar & oxoid dispenser |
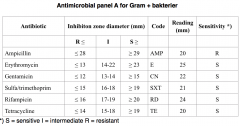
Hvordan?Gøres for begge kolonier —> Inocolum forberedes ved at overføre 5 kolonier til isotonisk saltvand. Her skal der opnås en uklarhed lig med MacFarland standard 0.5 (rør til sammenligning). Fugt en steril svaber i det netop lavede inokulum. Inokuler hele Müller Hinton agaren i 3 forskellige retninger for at sikre sammenflydende vækst. Sæt agar pladen ind under Oxoid disken og tryk på denne. Inkubation 37 °C. Der aflæses diameter størrelse for hver disk. Hvad?Oxoid disks A og C indeholder hver især forskellige antibiotika. Der testes herefter for om bakterien er sensitiv eller resistent over for antibiotikaen. Se skema 9. Resultater?se skemaer for resistensbestemmelse |
|
|
Resultater for resistensbestemmelse (G+) |
|
|
|
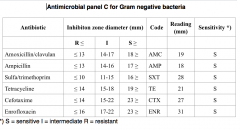
Resultater for resistensbestemmelse (G-) |
|
|
|
Bestemmelse af MIC-værdi ved agar fortynding
|
Hvordan?Der bruges 3 Müller-Hinton agar plader med hver især 2, 10 og 40 μg/ml tetracyklin. På disse podes inokulum der tidligere er lavet ved at lave en enkelt streg med et loop i. Inkubation 37°C. Hvad?MIC-værdien testes ved at teste bakteriens sensitivitet over for tetracyklin. Der hvor der skelner mellem vækst er MIC-værdien. Resultater?MIC-værdi > 2 μg/ml tetracyklin da der sås en lille smule vækst på denne plade. |
|
|
Forklar fermentation |
Document1 Fermentation er en anaerob nedbrydningsproces, hvor glukose nedbrydestil pyrodruesyre. Pyrodruesyre kan nedbrydes videre til forskelligeslutprodukter. Fermentation er uafhængig af ilt. |
|
|
Forklar oxidation |
Oxidation er en aerob nedbrydningsproces, hvor glukosens aldehydgruppeoxideres til en carboxylgruppe. Dette resulterer i dannelsen af glukonsyre.Oxidation er afhængig af ilt. |

