![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
64 Cards in this Set
- Front
- Back
|
Hva er den eneste aminosyren som ikke har et kiralt senter? |
Glycin, som har en R-sidegruppe med kun hydrogen. Hverken L eller D. Også Prolin er et unntak (iminosyre)som er en syklisk aminosyre, sidekjeden kovalent bundet til aminegruppen. Strengt tatt kiral |
|
|
Hvordan kan vi dele inn aminosyrer? |
Ikke polare, polare aminosyrer og etter sidegrupper ; alkyl( glycin, alanin, valin,metionin, leucin, isoleucin og prolin) , aromatisk ( fenylalanin, tryptofan), POLAR nøytral( serin, threonin, aspargin, glutamin, cystein og tyrosin), syrlig( aspartic acid, Glutamic acic), basisk ( histidin, lysin og arginin) |
|
|
Hva er navnet på aminosyrene? |
Glaciers in Alaska Victoriously Locate Isolated Prowlers ( Glycin, Alanin, Valin, Leucin, Isoleucin, Prolin)( alifatiske), Aroma of Pine, fine needles, Timber yellow and Trees with Wide trunks( Fenylalanin,f, Tyrosin y, Triptofan, w) Alcohol is a Serious(serin)Treat(Threonin), Basically History Loved kind Adventures roughly (Histidin, Lysin,Arginin Methodically (metionin) Check(cystein) for Sulfur, Acids (aspartat) Are Glue (glutamat) Amide this Neatly stacked Asparagus( aspargin) is Glutenous(glutamin) Quail |
|
|
Hva er løseligheten av et protein avhengig av? Hva skjer når du legger til et salt? |
Mengden av hydrofiliske aminosyrer som er tilstede i det spesifikke proteinet. Løseligheten synker og du kan få en utfelling (salting out). Mindre vannmolekylene til å reagere med proteinet når de reagerer med ladede ioner. |
|
|
Hva er og hva er målet med dialyse? |
Dialyse er en prosess hvor en separerer molekyler fra en semipermiabel membran. En kan bruke dette til å purifisere et protein for eks. |
|
|
Hvordan kan en separere proteiner basert på ladning? |
Ved å bruke "ion exchange chromatography" |
|
|
Hva kalles punktet der proteinet har en netto ladning= 0? |
Et isoelektrisk punkt. Er som regel forskjellig fra ulike aminosyrer. |
|
|
Beskriv peptidbindingen mellom 2 aminosyrer? |
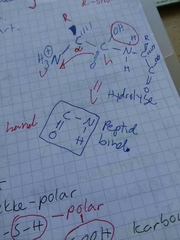
|
|
|
Hva hjelper ikke polare og polare aminosyrer med? |
Ikke polare aminosyrer hjelper i prosessen med å få proteinkjeder til å folde seg. Polare aminosyrer formerer hydrogenbindinger (-glycin) og fungerer som en nukleofil i en rekke enzymreaksjoner. |
|
|
Nevn et unntak fra en aminosyre? Hvordan dannes hitamin? |
Selenocystein kan dannes og dette blir ansett som en annen aminosyre enn de 20 andre. 2) Fra dekarboksylering av histidin og serotonin som kommer fra tryptofan. |
|
|
Hvordan addreserer en når et protein/molekyl roterer mot venstre eller høyre? |
L/D eller R/S systemet som fungerer bedre når en har molekyler med flere kirale senter. Hvordan en aminosyre roterer er avhengig av sidegruppen. |
|
|
Hvordan kan en studere absorbsjonen av ulik bølgelengde lys med proteiner? |
En kan bruke spektrometriske metoder. Aminosyrer absorberer ikke lys i det synlige spektrumet, abs. i ultrafiolett stråling og i infrarød spektrum. |
|
|
Hva er mekanismen bak en kan separere og analysere aminosyrer? |
En kan se på delingsegenskaper (partition) i forhold til dens evne til å assosiere med et løs. middel eller fase fremfor en annen. |
|
|
Hvordan er karboksylsyren og amidgruppen plassert i forhold til hverandre? |
Trans, siden dette gir minst sterisk hindring. |
|
|
Hvordan kan en definere et protein? |
Et molekyl som er satt sammen av en eller flere polypeptider. Med en kalles for monomerisk protein og med flere kalles det for et multimerisk protein. |
|
|
Hva stabiliserer i tertiære strukturer? Hva kjennetegner en kvartiæstruktur og hva kalles 2 peptidkjeder sammen? |
Hydrofobiske interreaksjoner er drivkraften, ioniske bind. , hydrogenbindinger også viktige. 2) To eller flere peptidkjeder sammen, kalles for et dimer. Holdt sammen av ioniske bindinger , van der wals, eller disuifidbindinger ( cystein) |
|
|
Hva bestemmer konformasjonen av et protein? Nevn en modifikasjon av aminosyrer? |
Aminosyre sekvensen. Ofte acylert ved enden (terminal) |
|
|
Trenger en å bryte en binding for å danne ulike konformasjoner? |
En kan rotere uten å bryte en binding, r/s strukturerbindinger |
|
|
Hva trenger en for å danne beta strukturer? |
Trenger vinkler (phi,psi) i korrekt rekkefølge. Hjelper sek. og tertiære strukturer. |
|
|
Hva er entalpieffekten? |
Det er når den polare delen av aminosyren blir plukket ut av hydrogenbindinger. Dette nedsetter totalenergien av systemet. |
|
|
Hva kan en si om antall proteinfoldinger fra et evolusjonært ståsted? |
At antall proteinfoldinger er limitert. |
|
|
Hva kan skje med et protein som du har tilføyd fri energi? |
Blir først denaturert, så aggredert. For å hindre aggredering så må proteinet komme beskyttet ut fra ribosomet slik at n terminus kan koble seg med c terminus. |
|
|
Hva skjer når proteinet utsettes for mer varme? |
Det blir produsert med varmesjokkproteiner. |
|
|
Hvilke to modeller beskriver resptorer som binder til proteiner? Hva trenger enzymer for å fungere? |
Lock and key model og induced fit model. 2) emzymer trenger kofaktorer. |
|
|
Hvilken aminosyre har den største konformasjonsfleksibiliteten på sin sidekjede? |
Lysin. |
|
|
Hvordan skiller en levende vs ikke levende organismer? Hva er konsekvensen av å ha ulike bindinger i et molekyl? |
Ved stoffmengden de inneholder og interreaksjonene mellom disse. 2) ulike bindinger har en effekt på geometrien til molekylet og reaktiviteten slik at energien er reflektert i bind. lengden på molekylet. |
|
|
Hva kan en si om ligander og sine tilhørende reseptorer? Hva kaller vi en levende organisme som ekstraherer energi fra kjemiske molekyler? |
Reseptorene til ligandene er stereospesifikke. 2) chemotrof. |
|
|
Hvordan er en proteinstuktur formert? |
Ved å folde en sekvens aminosyrer til en en 3dimensjonal figur. |
|
|
Hva er en viktig karakteristikk i forhold til aminosyrer og PH? |
Ved en PH rundt 7.4 så vil aminegruppen være positivt ladd og karboksylgruppen være deprotonert. Zwitterion |
|
|
Hvorfor er cystein interessant? |
Den kan bli oksidert når den er lokalisert ekstracellulært, danner disuifidbindinger som kalles "cystine". På intracellulært nivå blir cystein redusert. |
|
|
Hvrofor kalles lysin for snorklende? |
Fordi den kan oppføre seg både polart og upolart. |
|
|
Hva kaller vi det når flere sekundære proteinstukturer folder seg på en bestemt måte? Hva kalles det når flere av denne gruppen går sammen? |
Et motiv. Vanlig motiv er beta-alfa-beta motivet, som gjør det mulig å koble på er parallelt beta ark. 2) Flere motiv kan koble seg sammen og danne en kompakt globulær struktur, et domene. |
|
|
Hva er karakteristisk for en tertiærstruktur? |
Samler et arrangement helikser, beta ark og loops innen en enkel polypeptid. |
|
|
Hva er en Rossmann folding? |
Klassisk proteinfolding hvor en har alternerende beta tråder og alfa heliske segmenter. Beta trådene er foldet med hydrogenbindinger. |
|
|
Hva kalles hemoglobin? Hva kan en si om proteiner som var skapt senere evolusjonært? |
En tetramer. 2) At de utnyttet eksisterende foldninger istedenfor å finne nye. |
|
|
Hvorfor eksisterer det et limitert nummer av proteinfoldinger i naturen? |
Proteiner er modulære, forskjellige foldinger kombinerer for å skape mange forskjellige proteiner, proteiner fra høyt divergerende seksvenser kan ha den samme foldingen, det finnes antagelig et limitert antall stabile, funksjonelle proteinfoldinger, naturen bruker flesteparten av dem. |
|
|
Hva er de tre kreftene som driver proteinfolding? |
Hydrofobisk effekt, proteinene sin entalpi og proteinene sin konformasjonsentropi. En trenger et vannholdig omgivelser for primærfolding. |
|
|
Hva skjer med konformasjonsentropien ved proteinfolding? |
Den blir redusert. Totalt for systemet øker entropien siden vannmolekyler blir løst fra den hydrofobiske overflaten til proteiner. Hydrofobisk effekt. |
|
|
Hvorfor er en vannløsning så viktig ved proteinfolding? Hva er de to drivkraftene som promoterer en adopsjonen av en foldet konformasjon? |
Det er entropisk i favør å maskere hydrofobiske rester fra vann. 2) hydrofobiske effekten, nedsatt kjede konformasjonsentropi. |
|
|
Hva leder konformasjon til? |
Konformasjon er et produkt av imterreaksjonene til monomer enhetene den er satt sammen av og deres individuelle kjemiske egenskaper. |
|
|
Hva er styrken til de kovalente bindingene omvendt proporsjonalt med? |
Omvendt proporsjonalt med deres atomiske vekt. Eks H,O,N,C formerer de sterkeste kov. bindingene. |
|
|
Hvordan oppstår hydrofobiske reaksjoner? |
På bakgrunn av at vann heller vil reagere med seg selv enn upolare substanser. Disse interreaksjonene er spesielt viktige for å opprettholde membranstrukturen i cellene. Øker entropien til vann, vil heller danne polare bind. med seg selv. |
|
|
Hvor få gener trenger en organisme? |
Et minimum genmengde må kode for all informasjonen til cellulær metabolisme og informasjonen nødvendig for reproduksjon. |
|
|
Hvordan danner en supramolykulære komplekser? |
Når makromolekyler kommer sammen med ikke kovalente reaksjoner. |
|
|
Hvis H2O var lineær, hvilken egenskap ville den hatt? Hvordan kan en forklare at oppløsningen av ioniske komponenter av vann? |
Den ville vært en ikke polar substans. Den polare iltrekningen mellom løs. middel + løs. er større enn de intermolekylære kreftene i løs.-løs. |
|
|
Hva er en dielektrisk konstant? |
Forklarerer muligheten til et stoff å lagre potensiel elektrisk energi i et elektrisk felt. |
|
|
Hva kaller vi den strukturen H2O formerer rundt rundt en løsning? |
Det hydrogen bundet H2O nettverket danner en kladratstruktur rundt løsningen. Klatrat er en kjemisk struktur som har en annen kjemisk struktur innesluttet i hulrommet av krystallstrukturen. |
|
|
Hvordan er essensielt entropi? |
En økning i mikrotilstander i et makrosystem. Analogt hvis en makrotilstand kun er representert av en mikrotilstand, så har systemet ingen frihet til å velge sin mikrotilstand = 0 entropi. |
|
|
Hva er foskjellen mellom konfigurasjon og konformasjon? |
Med konfigurasjon så er det den permanente strukturen gitt av molekylet. Må bryte bindinger for å danne den. Med konformasjon så skiller dette den romslige orienteringen et molekyl kan oppnå. |
|
|
Hva gjør en for å øke entropien for aminosyrer? |
En setter den ikke polare delen på innsiden og den polare delen på utsiden. |
|
|
Hva referer til at antall proteinfoldinger er limitert? Hva referer maks enzym hurtighet til? |
Levinthals paradoks. Tilstanden der alle de aktive setene er fylt opp. Hvis det finnes mer substrat enn # mulige seter, så kan du ikke øke hurtigheten på reaksjonen mer enn alle setene er fylt opp. |
|
|
Hvor skjer blodkoaguleringen? Hva er blodproper laget av? |
Inni blodkar. Fibrin og blodplater |
|
|
Hvor kommer blodplater fra? |
Blodplater er cellulære fragmenter uten cellekjerne som kommer fra beinmargen celler kalt for mega-karyocites. Fibrin hjelper å stabilisere blodplate pluggen. |
|
|
Hva heter de tre fasene av blodplate formasjon? |
Initiering, ekstensjon og stabilisering. |
|
|
Hva får blodplater til å strømme til skaden i blodkaren og leder til dannelse av en blodpropp? Hvs skjer umder ekstensjonsfasen? |
Von Willebrand faktoren. Initiering 2) flere blodplater kommer til og det dannes et blod aggregat. |
|
|
Hvordan blir blodplater aktivert? |
Kollagen, thrombin, ADP og thromboxam A2 |
|
|
Hva er lipotoksisitet? |
En giftig effekt av fett på celler. Leder til cellulær udrift og apoptosis. |
|
|
Hva kaller vi for lipolyse? |
Den første prosessen med å mobilisere lipider hvor bindingen mellom fettsyrene og glycerol blir brutt. |
|
|
Beskriv de 3 trinnene i lipolyse? |
Tri-acyl-glycerol blir konvertert til di-acyl-glycerol gjennom lipasen ATGL, så fra di til mono acyl glyserol med enzymet HSL. Siste trinnet bli glyserol delt fra fettsyrene med MGL |
|
|
Hvordan kan fettsyrer bli transportert i det hydrofile cytosol? |
Ved hjelp av FABP4 som fungerer som en chaperon. |
|
|
Hvor er elektron transportkjeden lokalisert i celler? Beskriv chemioosmotisk teori? |
Intermembran området. 2) En har en exergonisk overførsel av elektroner som gir energi til overførselen av protoner til inter membranrommet. Protoner flyter ned deres kons. gradienten for å gi energi til den endergoniske syntesen av ATP. |
|
|
Beskriv Levinthals paradoks? Hva er en grunn til at proteiner kan raskt finne sin "native conformation"? |
Et protein ville essensielt aldri funnet sin native fold med å gå igjennom alle variasjonene. 2) Eksisterer en høy grad av samarbeid i proteinfolding. |
|
|
Hva er katalyse? |
Katalyse er når noen stoffer øker hastigheten av kjemiske reaksjoner uten å være en del av selve reaksjonen. |
|
|
Hvilket protein kutter prothrombin? Er følgende proteiner intrinsic eller extrinsic (Faktor xII, faktor VII, eller tissie factor?) |
Faktor X. 2) faktor xII- intrinsic, faktor vII- intrinsic, TF- extrinsic. |

