![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
12 Cards in this Set
- Front
- Back
|
Définition : Solution aqueuse |
Mélange liquide dans lequel l'eau constitue le solvant, c'est a dire qu'elle est en excès par rapport aux autres soluté |
|
|
Les pouvoirs de l'eau |
-hydratant -ionisant -dissociant -dispersant |
|
|
La conductivité des solutions aqueuses |
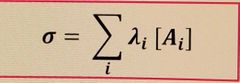
|
|
|
Les mesures conductimétrique |
On ne peut pas mesurer directement la conductivité d'une solution électrolytique, ni celle d'une espèce ionique En revanche on peut accéder à la résistance R (en ohm) d'une portion de la solution et donc a la conductance G (en ohm ou en sieverts) |
|
|
Formule qui lie R a G |
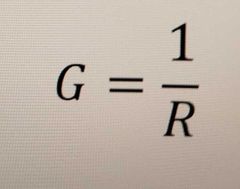
|
|
|
Formule de G en fonction des électrodes |
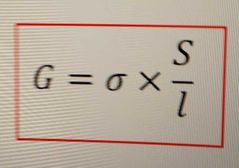
|
|
|
L'activité d'un soluté |
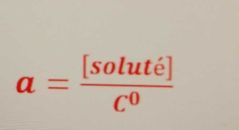
Dans une solution diluée (c<10**-2 mol)
|
|
|
Formule du Quotient de réaction |
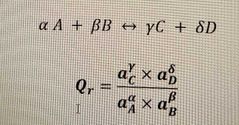
|
|
|
Qr et K |
Quand Qr = k : système a l'équilibre Quand Qr < k : sens direct Quand Qr > k : sens indirect |
|
|
Définition : électrolyte fort |
Totalement dissocié Expl : HCL n'existe pas dans l'eau |
|
|
Définition électrolyte faible |
Partiellement dissocié on parle d'équilibre Expl : CH3COOH existe toujours dans l'eau |
|
|
Acide et base selon Bronsted-Lowry |
-Un acide est un donneur de proton CH3COOH --> CH3COO- +H -Une base est un accepteur de proton CH3COO- +H --> CH3COOH |

