![]()
![]()
![]()
Use LEFT and RIGHT arrow keys to navigate between flashcards;
Use UP and DOWN arrow keys to flip the card;
H to show hint;
A reads text to speech;
40 Cards in this Set
- Front
- Back
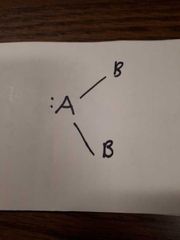
Nommer la structure moléculaire géométrique |
Trigonale plan Angulaire, 3 voisins, AX2E1, 1 doublet libre M< = ~120° |
|

Nommer le type de structure géométrique |
Linéaire, 2 voisins AX2, 0 doublet libre m< = 180° |
|
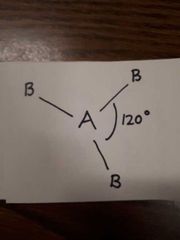
Nommer le type de structure moléculaire géométrique |
Trigonale plan, 3 voisins AX3, 0 doublet libre m<= 120° |
|

Nommer le type de structure moléculaire géométrique |
Octaédrique Plane carrée, 6 voisins AX4E2, 2 doublets libres m<= 90° |
|
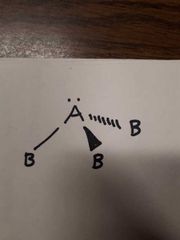
Nommer le type de structure moléculaire géométrique |
Tétraédrique Trigonale pyramidale (ou pyramide à base triangulaire) 4 voisins AX3E1, 1 doublet libre m<= ~ 109° |
|
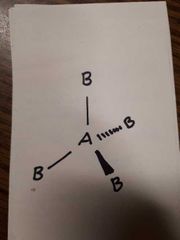
Nommer le type de structure moléculaire géométrique |
Tétraédrique 4 voisins AX4, 0 doublet libre m<= 109° |
|
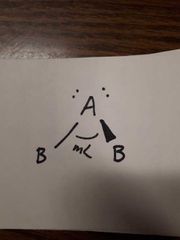
Nommer le type de structure moléculaire géométrique |
Tétraédrique, Angulaire 4 voisins AX2E2, 2 doublets libres m<= ~ 109° |
|
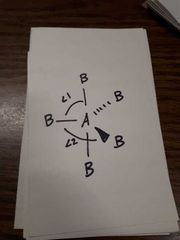
Nommer le type de structure moléculaire géométrique |
Trigonale bipyramidale (bipyramidale à base triangulaire) 5 voisins AX5, 0 doublet libre m<1= 90° m<2= 120° |
|
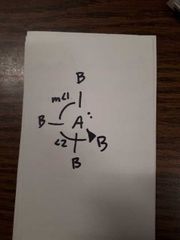
Nommer le type de structure moléculaire géométrique |
Trigonale bipyramidale À bascule ou balançoire 5 voisins AX4E1, 1 doublet libre m<1= ~90 m<2=~ 120° |
|
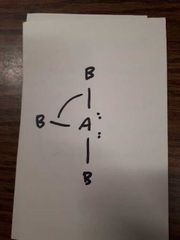
Nommer le type de structure moléculaire géométrique |
Trigonale bipyramidale Forme de T 5 voisins AX3E2, 2 doublets libres m<= ~90° |
|

Nommer le type de structure moléculaire géométrique |
Trigonale bipyramidale Linéaire 5 voisins AX2E3, 3 doublets libres m<= 180° |
|

Nommer le type de structure moléculaire géométrique |
Octaédrique (bipyramidale à base carré) 6 voisins AX6, 0 doublet libre m<= 90° |
|

Nommer le type de structure moléculaire géométrique |
Octaédrique Pyramidale à base carrée 6 voisins AX5E1, 1 doublet libre m<= ~90° |
|
|
Vrai ou faux? Les doublets libres créent plus de répulsion que les doublets liés? |
Vrai |
|
|
Quels sont les éléments les plus électronégatifs? |
Oxygène, Azote, Halogènes (F, Cl...) |
|
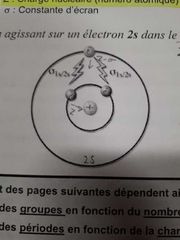
Qu'est ce que l'effet d'écran? |
Diminution de l'attraction entre le noyau et l'électron de valence à cause des électrons de coeur |
|
|
Vrai ou faux? Le rayon atomique est le double de la distance entre 2 noyaux |

Faux c'est la moitié de la distance entre 2 noyaux |
|
|
Expliquer l'effet du rayon atomique dans une période (de gauche à droite) |
Le rayon atomique diminue dans une période de gauche à droite parce qu'il y a le même nombre d'électrons de coeur Il y a de plus en plus de protons, ce qui raptisse le nuage électronique (+++ attraction) |
|
|
Expliquer l'effet du rayon atomique dans un groupe (de haut en bas) |
Le rayon atomique augmente dans un groupe puisque les orbitales sont de plus en plus gros. Donc tout le monde est plus éloigné les uns des autres. |
|
|
Vrai ou faux? La taille d'un atome qui devient un cation est plus petit que lorsqu'il est neutre? |
Vrai, il y a moins d'électrons, donc moins de compétition, donc plis attraction |
|
|
Vrai ou faux? La taille d'un atome qui devient un anion est plus petit que lorsqu'il est neutre? |
Faux , puisqu'il gagne un électron, les électrons ont plus de compétition, donc il y a plus de répulsion (les électrons prennent plus d'espace), ce qui fait en sorte que le nuage électronique est plus grand |
|
|
Comment déterminer quel ion possede le nuage électronique le plus petit. Ex: Mg2+, O2- , F- , Na+ |
Il faut regarder qui a le plus de protons (à l'aide du tableau périodique) puisque les protons permettent l'attraction entre ceux-ci et les neutrons |
|
|
Vrai ou faux? L'énergie d'ionisation est l'énergie nécessaire pour arracher l'électron le plus faible dans un atome? |
Vrai L'énergie de première ionisation est l'énergie nécessaire pour arracher le 1er électron L'énergie de deuxième ionisation est l'énergie nécessaire pour arracher le 2eme électron le plus faible Ect... |
|
|
Décriver l'effet de l'énergie d'ionisation dans une période (de gauche à droite) |
L'énergie d'ionisation augmente dans une période. Le nombre de protons, ce qui cause une attraction plus forte entre électrons et protons. Donc l'énergie pour les séparer est de plus en plus élevée. |
|
|
Décrivez la valeur de l'énergie d'ionisation dans un groupe (de haut en bas) |
L'énergie d'ionisation diminue dans un groupe puisque les orbitales sont plus gros. Les électrons sont beaucoup plus éloignés des protons, donc l'énergie pour les séparer est faible |
|
|
Nommer les propriétés des métaux que les non-métaux ne peuvent pas avoir |
- malléable - ductile - bon conducteur thermique et électrique - facilité à donner des électrons |
|
|
Décrivez la différence entre une liaison covalente et ionique |
Liaison covalente : partage d'électrons entre non-métaux Peut être chargé (polaire) Liaison ionique : transfert d'électrons entre métaux et non-métaux (Non polaire) |
|
|
Qu'est ce que l'électronégativité? |
La tendance qu'à un atome à attirer vers lui les électrons d'une liaison covalente |
|
|
Quelle est la différence entre une liaison covalente polaire et non polaire |
Liaison covalente polaire: inégalité entre le partage d'électrons des 2 atomes, un est plus électronégatif que l'autre Liaison covalente non polaire: Égalité dans le partage d'électrons, les atomes sont électronégativement semblabes |
|
|
Polaire? Non polaire? Ionique? A) si électronégativité = 0 B) si électronégativité < 0,5 C) si électronégativité = 1,7 D) si électronégativité = 3,2 |
A) liaison covalente (non-polaire) B) liaison covalente (non-polaire) C) liaison covalente (polaire) D) liaison ionique |
|
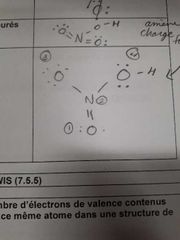
Donner l'équation de la charge formelle |
Cf = nb d'é de valence seuls - nb d'é doublet libre - nb de liaison *doit être le plus près de zéro* |
|
|
Qu'est ce qu'un octet incomplet? |
Atome central entouré de moins de 8 électrons (Be, B, Al) |
|
|
Qu'est ce qu'un octet étendu? |
Éléments de la 3eme période et plus bas que peuvent posséder plus de 8 électrons |
|
|
Qu'est ce que un radicaux |
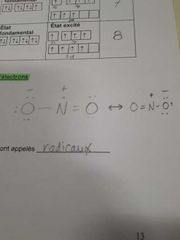
Composés qui contiennent un électron non-apparié |
|
|
Quelle type de force moléculaire retrouve-t-on Entre des molécules non-polaire? |
Force de dispersion |
|
|
Quel type de force moléculaire retrouve-t-on Entre des molécules non-polaire et polaire? |
Force diplôle-diplôle induit Force de dispersion |
|
|
Quel type de force moléculaire retrouve-t-on Entre des molécules polaires? |
Force diplôle-diplôle Force dispersion Liaison hydrogène (dépend) |
|
|
Quel type de force moléculaire retrouve-t-on Entre des molécules polaires ou non-polaire et des ions? |
Force ion-dipôle Force ion-dipôle induit Force dispersion |
|
|
Quelles sont les 2 facteurs qui détermine qu'une liaison hydrogène peut être appliqué? |
1. Doit être lié à N, O, F 2. Doit se lier à N, O, F |
|
|
Est ce que cette équation est vraie? I1 > I2 > I3 |
Elle est fausse, puisque l'énergie nécessaire pour séparer le 1er électron est plus faible que celle nécessaire pour le 2 eme électron |

